新闻发布
ITK抑制剂soquelitinib临床数据亮眼,或成“自免药王” Dupixent最强对手
ITK抑制剂soquelitinib(CPI-818)针对中重度特应性皮炎的美国临床1期队列4的数据于北京时间1月20日晚间公布。与队列1-3的4周治疗相比,8周治疗显示了更积极的疗效和安全性结果:75%的患者达到EASI 75,25%达到EASI 90,33%达到IGA 0/1。在既往接受过Dupixent单抗和JAK抑制剂的患者,60%达到EASI 75。该突破性数据表明,soquelitinib有潜力成为一种用于中重度特应性皮炎患者一线治疗的重要新药,凭借其“源头干预、安全口服、面向难治”的差异化优势,有望成为当前“自免药王”Dupixent的最强竞争对手。
来自特应性皮炎1期临床试验的队列4数据
截至2026年01月15日,队列4的入组已完成,所有接受soquelitinib治疗的患者(n=12)均完成了56天的疗程。在12名入组的安慰剂患者中,有10名在第56天可评估,因为2名患者错过了第56天的访视;这两名患者在之后的时间点完成了计划外随访。
队列4患者与队列3的患者具有相似的基线特征,与队列1和2的患者相比,这些队列的患者疾病更严重,平均基线EASI(湿疹面积与严重程度指数)评分更高。队列4中,接受soquelitinib治疗的患者平均基线EASI为25.7,接受安慰剂治疗的患者为21.9。
图1总结了队列1至4评估EASI 75、EASI 90和IGA 0,1的疗效结果。队列3和4的结果看起来相似,但队列4达到EASI 75和90的比例更高。对于队列4,接受soquelitinib治疗的患者分别有75%、25%和33%达到EASI 75、EASI 90和IGA 0/1,而安慰剂组则分别为20%、0%和0%。
图1:在治疗第28天(队列1-3)或第56天(队列4)达到终点EASI 75、EASI 90和IGA 0或1的患者百分比
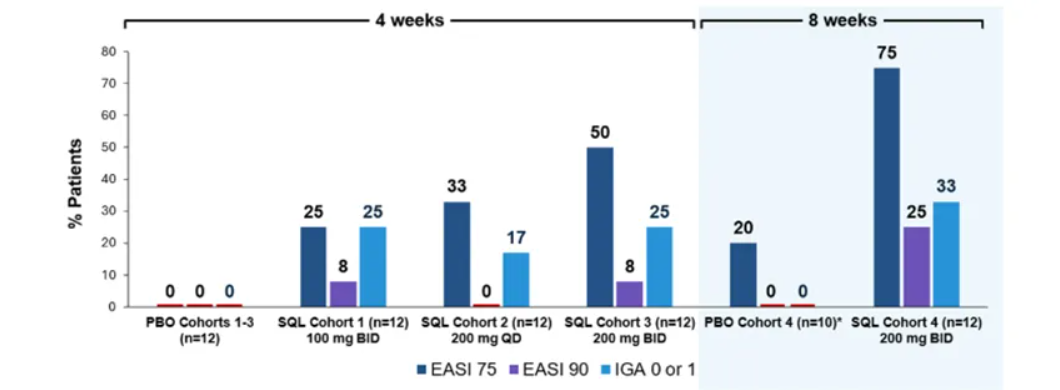
图2显示了队列4接受soquelitinib和安慰剂患者的反应动力学。曲线在首次访视(第15天)就出现分离,并持续增加到第56天。第56天结果差异具有统计学显著性,p=0.035。疾病控制在30天治疗后的随访期内得以维持。
图2:队列4平均EASI降低百分比
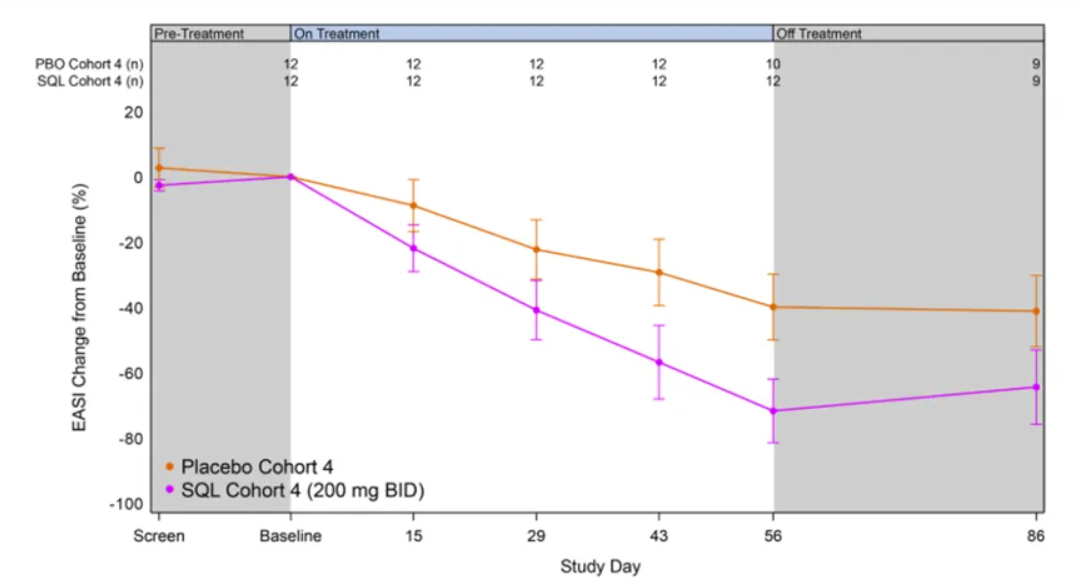
图3A和3B显示了队列1-4所有患者以及仅队列3-4患者中接受soquelitinib和安慰剂患者的反应曲线,按是否曾接受过全身治疗进行了亚组细分。在所有4个队列中,有25名患者(占所有患者的35%)既往接受过全身治疗,其中度普利尤单抗是最常见的既往全身疗法(n=11),其他既往全身疗法包括JAK抑制剂、皮质类固醇和研究性药物。无论既往全身治疗史如何,接受soquelitinib治疗的患者的反应曲线大致相同。与未接受过全身治疗的安慰剂患者相比,曾接受过全身治疗的安慰剂患者的EASI降幅较小。这些结果证明soquelitinib在全身治疗初治患者和有经验的患者中具有相似的活性。另外,有既往全身治疗经验的患者似乎疾病更严重。两名达到EASI 75的安慰剂患者未接受过既往全身治疗。七名接受过全身治疗的安慰剂患者中,没有一人达到EASI 75或EASI 50;而5名接受过全身治疗的soquelitinib治疗患者中,有3名达到了EASI 75。
图3:队列1-4平均EASI降低百分比——按是否曾接受全身治疗分组的患者细分
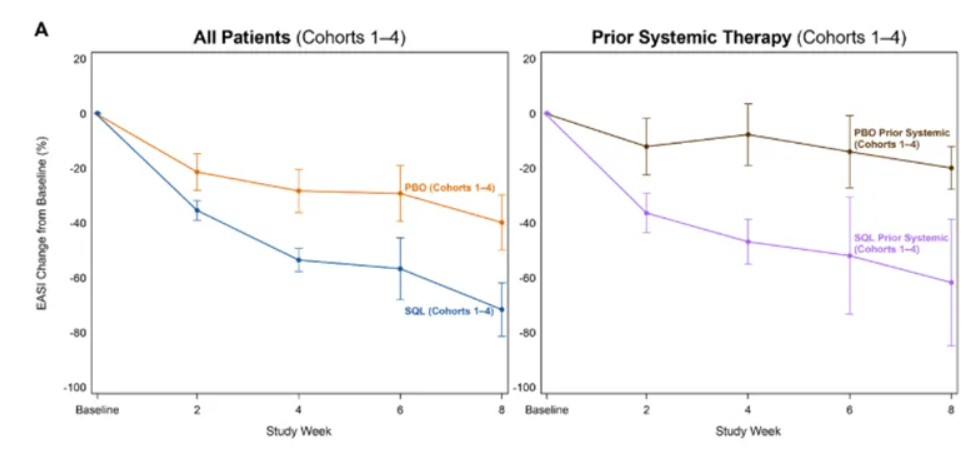
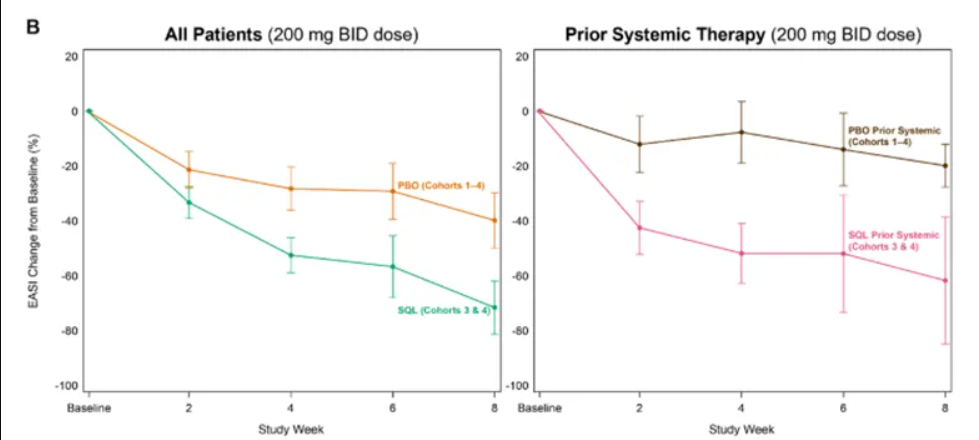
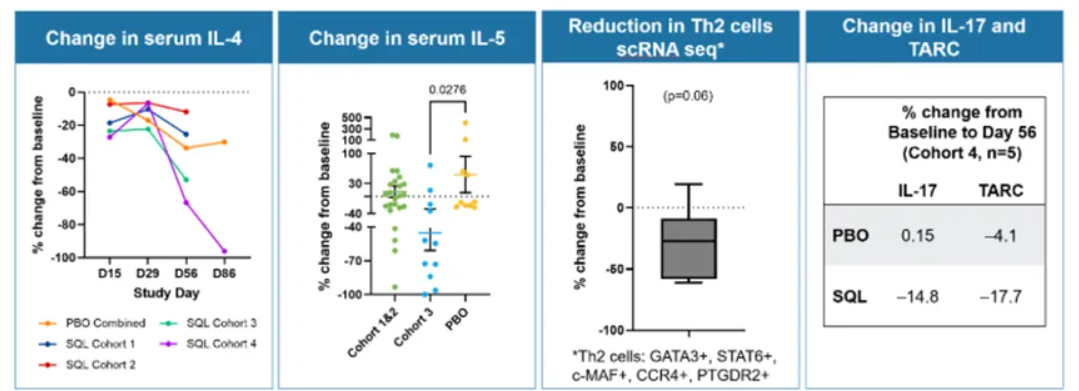
图4显示了同样接受200 mg bid的队列3患者的更长期随访数据。数据显示,在治疗期结束后长达3个月的时间内,EASI评分得到维持或改善,并且循环Treg细胞增加。
图4:队列3平均EASI降低百分比及队列1-3的Treg细胞百分比变化
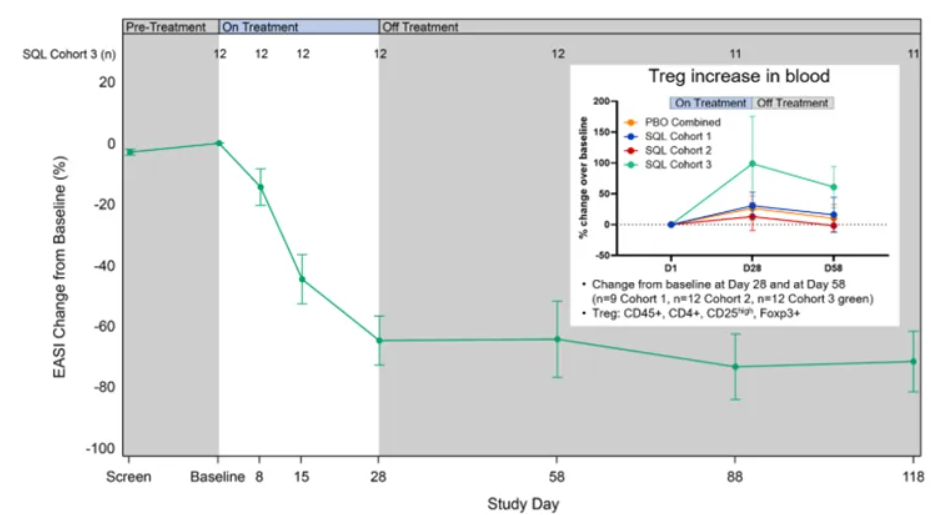
生物标志物数据见图5。在队列3和4中观察到血清IL-4细胞因子水平降低,无论是在治疗期间还是治疗后期间,且呈剂量依赖性反应,队列4患者显示直至第86天的IL-4降幅最大。来自队列1-3的生物标志物数据显示,与安慰剂相比,队列1-3的血清IL-5细胞因子水平降低,包括呈剂量依赖性反应,队列3患者与安慰剂相比显示IL-5降幅最大。血清IL-5的降低早在治疗第8天就已出现。血清IL-17和TARC水平也较低。通过scRNA测序技术测量了循环Th2细胞(n=6,来自队列1和2),并证明这些细胞随治疗而减少。如上所述,队列3患者的循环Treg细胞增加,并与延长的治疗效果相关。这些结果与观察到的soquelitinib阻断Th2和Th17细胞及其分泌的细胞因子(如IL-4、IL-5、IL-17)的能力以及对T reg细胞的影响相一致。这些生物标志物数据表明,soquelitinib诱导了涉及Th1、Th2、Th17和Treg细胞的免疫系统再平衡。
图5:生物标志物数据:血清IL-4、IL-5、IL-17、TARC的变化及Th2细胞的减少
队列4的安全性数据
截至2026年1月15日,未观察到新的安全信号。报告的不良事件发生在41.7%的soquelitinib患者和50%的安慰剂患者中;所有均为1-2级,且未导致任何剂量调整或中断。未报告严重或严重不良事件。未发现明显的实验室异常。
您也可以通过以下链接查阅相关信息:
https://corvuspharma.gcs-web.com/news-releases/
※ 关于特应性皮炎
特应性皮炎又称湿疹,是一种慢性疾病,可引起皮肤炎症、红斑、鳞屑、水疱和刺激症状。目前的治疗方法包括局部用药、口服用药和全身注射生物制剂疗法。特应性皮炎经常与食物过敏和哮喘等其他过敏性疾病相关。特应性皮炎与哮喘和过敏一样,都有Th2淋巴细胞的参与,它们分泌的细胞因子会导致炎症。临床前研究表明,soquelitinib能抑制Th2淋巴细胞产生细胞因子。中国有超过6500万特应性皮炎患者,其中近28%为中重度患者。预计到2030年,市场规模将超过40亿美元。
※ 关于Soquelitinib
Soquelitinib(CPI-818)是处于临床阶段的具有高选择性的口服小分子ITK抑制剂。ITK主要在T细胞中表达,在T细胞和自然杀伤(NK)细胞的免疫功能中发挥作用。研究表明,soquelitinib能影响T细胞分化,诱导Th1辅助细胞的生成,同时阻断Th2和Th17细胞的发育及其分泌细胞因子的产生。Th1细胞是肿瘤、病毒感染和其他传染性疾病免疫所必需的。Th2和Th17辅助性T细胞参与了许多自身免疫性和过敏性疾病的发病机制。公司相信,抑制 T 细胞中的特定分子靶点可能对癌症(包括实体瘤)患者以及自身免疫性和过敏性疾病患者有治疗效果。最近的研究表明,ITK 控制着 Th17(炎症促进细胞)和调节性T细胞(炎症抑制细胞)之间的转换。抑制 ITK 会促使T细胞向调节性T细胞转化,从而有可能抑制自身免疫和炎症反应。2024年12月,npj Drug Discovery杂志刊登了一篇介绍soquelitinib的化学、酶学和生物学的最新论文。
※ 关于和剂药业
和剂药业是一家专注于免疫调节创新疗法的生物医药公司,致力于通过靶向T/B细胞关键信号通路,开发突破性药物以改善癌症、自身免疫病及炎症性疾病的治疗。公司由贝达基金、海正药业、泰格医药、檏盛投资共同投资,并与美国Corvus Pharmaceuticals (CRVS)达成战略合作。欲了解更多信息,请访问 www.angelpharma.com。
